消費者庁で検討が進む機能性表示食品制度の「対象範囲拡大」が"ゼロ回答"となる恐れが出てきた。4月末の第4回会合も反対派のペースで議論が進行。もっとも市場性のある「ビタミン・ミネラル」が対象とならない可能性がある。よくて「脂質」や「糖質・糖類」まで。ただ、これは昨年4月の制度開始時の設計上のミスを正す、いわば微修正に過ぎない。否定的見解で一貫する消費者サイドに序盤戦で議論が煮詰まる中、日本通信販売協会から検討会に参加する宮島和美理事から法整備を求める意見が飛び出した。
〝ゼロ回答〟の恐れ 検討会は序盤戦を終え、業界は明らかに劣勢だ。対象化の議論が進むのは、「食事摂取基準に規定される栄養成分等(ビタミン・ミネラル、糖質・糖類、脂質、たんぱく質等)」。ただ、ビタミン・ミネラルの過剰摂取に関する懸念を示した食品安全委員会の「いわゆる『健康食品』に関するメッセージ」で示された安全面の懸念、食事摂取基準を前提に整備された「栄養機能食品」との混同の恐れなど整合性の観点から対象化は時期尚早との意見が強い。
「座長」も反対派?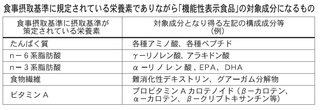
"劣勢"は当然の結果でもある。検討会メンバーは17人。このうち昨年の食事摂取基準改定に関わった委員が2人(寺本民生座長、佐々氏敏氏)、「メッセージ」策定に関わった委員が6人(梅垣敬三座長代理、合田幸広氏、吉田宗弘氏、河野康子氏、迫和子氏、戸部依子氏)。
業界サイドを除き過半を占め、検討会を仕切る座長、座長代理からして対象化に懸念を持つ陣容だ。これら委員に自らが関与した「メッセージ」の自己批判を求め、対象化をめざすこと自体無理がある。
第4回会合では「糖質・糖類」の一部は「一定の条件下で対象化も可能では」(吉田委員)といった意見も出た。ただ、「糖質」等は本来、制度導入の段階で"栄養素との作用の違い"を前提に制度に使用可能な成分
(表㊨)にされるべきだったもの。「範囲拡大」の成果とは言い難い。
反対派を追認
消費者庁の狙いも透けてみえる。第4回会合では「議論にあたっての基本的な考え方」と題する3項目の留意点を提示。その中で「関連諸制度や関連行政機関の知見との整合性を考慮すべき」と触れた。「関連する諸制度」とは栄養機能食品のこと、「関連行政機関の知見」は「メッセージ」などを指す。反対派の意見を追認するような内容に「これでは(範囲拡大を)やりませんと言っているのと同じ」と傍聴者の一人は落胆する。
「法制化で合意を」 そんな中、第4回会合では、宮島委員から「(個々の栄養成分の精査など)各論も大事だが『サプリメント法』が制定されるべきと思う。きちんとした法律のもとで運用されることが大事」との発言があった。その真意を巡り、さまざまな声があがっている。
ある傍聴者は「突然の発言で真意が分からなかった」と漏らす。
一方、別の傍聴者は「法律がないから46通知などさまざまな規制との整合性が度々俎上に上がる。『届出制』にも関わらず実質『審査』のような運用もされる。その都度ひと悶着起こり遅々として制度が浸透しない。検討会で法制化の合意を形成すべき」と、同調する。
実際、届出を行った企業は「以前は通った届出文言が今では通らない」など、消費者庁の判断基準のあいまいさを指摘する。運用実態が「審査」に傾くのも法整備が不十分で裁量が入り込む余地が大きいからだ。
◇
「法制化」という大局的な視点は、その突破口になる可能性がある。
政府は、制度の目的にを「健康長寿社会の延伸」と「成長産業の育成」の両立と明確にしている。だが検討会の議論はこれに逆行。「栄養機能食品」との整合性など枝葉末節にこだわり、新制度の確立に向けた議論は一向に進まない。
「法制化」議論の中で国の健康・栄養政策を明確にし、これまで場当たり的に整備してきた諸制度の見直しを進める必要があるのではないか。法制化の合意形成で継続的な議論の土台をつくる必要がある。
規制改革会議の森下竜一氏に聞く「検討会の行方と新制度の評価」「対象拡大」が大前提、〝どう入れるか〟を議論すべき
機能性表示食品制度導入のキーマンとして規制改革会議委員を務める森下竜一大阪大学大学院教授に新制度の評価を聞いた。(聞き手は本紙記者・佐藤真之)
――「対象成分の範囲」を議論する消費者庁の積み残し課題検討会をどう見ている。
「当然、範囲を拡大するべきだと考えている」――消費者サイドの反発も根強い。
「消費者サイドの反発は、あまり認識していない。もともと範囲を拡大する観点での検討会だと認識している。消費者の理解をえられるように、どのように制度に入れるかが議論のポイントのはずだ。『関与成分が不明確なもの』は漢方も同じ。医薬品として品質管理できているものを入れない理由が分からない」――漢方や「栄養機能食品」(栄機)で扱えばよいという意見もある。
「『機能性表示食品』はあくまで健康の維持増進の立場から扱うものであるし、漢方の新規承認として、という話とは全く筋が違う。また、国が管理し、厳密な機能性評価で定型文を表示する『栄機』とは設計が異なる。新たな知見、根拠が得られているのであれば企業責任で表示すればいい。それに実態として『栄機』は自主認証で全体の把握が難しい。届出を行い、情報公開される新制度の方が透明性は高い。消費者にとっても、そちらの方がメリットは大きい」
――規制改革会議としてこれまでの議論をどう見ている。
「(範囲拡大とならなければ)当然、会議でも議論させてもらう。ただ今の会議体は7月まで(※)。メンバーの留任・変更は決まっていないが、いずれにしても重点的なフォローアップ案件として申し送りしたい」――改善すべき点は。
「生鮮食品の受理はわずか3商品。もう少しスムースに届出が行えるよう次回の制度改定でサプリメントと別枠にして、実情に応じた制度にすべきだと考えている」――制度の評価は。
「産業界、消費者サイドともウィンウィンになったのではないか。企業は機能が表示でき、情報公開されることで消費者団体はその内容をチェックできる。透明性が増したのは間違いない。議論を行う素地ができた」
「ただ今の制度運用は届け出のはずなのに、実質『審査』になっていないか危惧している。判断基準もあいまいに思える。しかも受理にかかる時間が遅い点は危惧している。制度の本来の趣旨である『企業責任』のベースに基づいて考えるべき」
――「チアフル酵母」の届出撤回を巡る問題の見解は。
「(届出の撤回が)仕方ないとは思わない。食品に含まれる成分でもあり、46通知の規制対象から新制度は除外されている。46通知の『専ら医薬品リスト』から外すことを検討してもよい成分もあり、次の規制改革会議では食薬区分の見直しも申し送り事項としたい。制度の狭間の問題を解決しないといけない」
――受理件数(300件)に対する評価は。
「少なすぎる。年内に1000商品は必要ではないか」 ※規制改革会議は、7月の参院選後、新たな会議体として発足する予定。









〝ゼロ回答〟の恐れ
検討会は序盤戦を終え、業界は明らかに劣勢だ。対象化の議論が進むのは、「食事摂取基準に規定される栄養成分等(ビタミン・ミネラル、糖質・糖類、脂質、たんぱく質等)」。ただ、ビタミン・ミネラルの過剰摂取に関する懸念を示した食品安全委員会の「いわゆる『健康食品』に関するメッセージ」で示された安全面の懸念、食事摂取基準を前提に整備された「栄養機能食品」との混同の恐れなど整合性の観点から対象化は時期尚早との意見が強い。
「座長」も反対派?
業界サイドを除き過半を占め、検討会を仕切る座長、座長代理からして対象化に懸念を持つ陣容だ。これら委員に自らが関与した「メッセージ」の自己批判を求め、対象化をめざすこと自体無理がある。
第4回会合では「糖質・糖類」の一部は「一定の条件下で対象化も可能では」(吉田委員)といった意見も出た。ただ、「糖質」等は本来、制度導入の段階で"栄養素との作用の違い"を前提に制度に使用可能な成分(表㊨)にされるべきだったもの。「範囲拡大」の成果とは言い難い。
反対派を追認
「法制化で合意を」
そんな中、第4回会合では、宮島委員から「(個々の栄養成分の精査など)各論も大事だが『サプリメント法』が制定されるべきと思う。きちんとした法律のもとで運用されることが大事」との発言があった。その真意を巡り、さまざまな声があがっている。
ある傍聴者は「突然の発言で真意が分からなかった」と漏らす。
一方、別の傍聴者は「法律がないから46通知などさまざまな規制との整合性が度々俎上に上がる。『届出制』にも関わらず実質『審査』のような運用もされる。その都度ひと悶着起こり遅々として制度が浸透しない。検討会で法制化の合意を形成すべき」と、同調する。
実際、届出を行った企業は「以前は通った届出文言が今では通らない」など、消費者庁の判断基準のあいまいさを指摘する。運用実態が「審査」に傾くのも法整備が不十分で裁量が入り込む余地が大きいからだ。
◇
「法制化」という大局的な視点は、その突破口になる可能性がある。
政府は、制度の目的にを「健康長寿社会の延伸」と「成長産業の育成」の両立と明確にしている。だが検討会の議論はこれに逆行。「栄養機能食品」との整合性など枝葉末節にこだわり、新制度の確立に向けた議論は一向に進まない。
「法制化」議論の中で国の健康・栄養政策を明確にし、これまで場当たり的に整備してきた諸制度の見直しを進める必要があるのではないか。法制化の合意形成で継続的な議論の土台をつくる必要がある。
規制改革会議の森下竜一氏に聞く「検討会の行方と新制度の評価」
「対象拡大」が大前提、〝どう入れるか〟を議論すべき
――「対象成分の範囲」を議論する消費者庁の積み残し課題検討会をどう見ている。
「当然、範囲を拡大するべきだと考えている」
――消費者サイドの反発も根強い。
「消費者サイドの反発は、あまり認識していない。もともと範囲を拡大する観点での検討会だと認識している。消費者の理解をえられるように、どのように制度に入れるかが議論のポイントのはずだ。『関与成分が不明確なもの』は漢方も同じ。医薬品として品質管理できているものを入れない理由が分からない」
――漢方や「栄養機能食品」(栄機)で扱えばよいという意見もある。
「『機能性表示食品』はあくまで健康の維持増進の立場から扱うものであるし、漢方の新規承認として、という話とは全く筋が違う。また、国が管理し、厳密な機能性評価で定型文を表示する『栄機』とは設計が異なる。新たな知見、根拠が得られているのであれば企業責任で表示すればいい。それに実態として『栄機』は自主認証で全体の把握が難しい。届出を行い、情報公開される新制度の方が透明性は高い。消費者にとっても、そちらの方がメリットは大きい」
――規制改革会議としてこれまでの議論をどう見ている。
「(範囲拡大とならなければ)当然、会議でも議論させてもらう。ただ今の会議体は7月まで(※)。メンバーの留任・変更は決まっていないが、いずれにしても重点的なフォローアップ案件として申し送りしたい」
――改善すべき点は。
「生鮮食品の受理はわずか3商品。もう少しスムースに届出が行えるよう次回の制度改定でサプリメントと別枠にして、実情に応じた制度にすべきだと考えている」
――制度の評価は。
「産業界、消費者サイドともウィンウィンになったのではないか。企業は機能が表示でき、情報公開されることで消費者団体はその内容をチェックできる。透明性が増したのは間違いない。議論を行う素地ができた」
「ただ今の制度運用は届け出のはずなのに、実質『審査』になっていないか危惧している。判断基準もあいまいに思える。しかも受理にかかる時間が遅い点は危惧している。制度の本来の趣旨である『企業責任』のベースに基づいて考えるべき」
――「チアフル酵母」の届出撤回を巡る問題の見解は。
「(届出の撤回が)仕方ないとは思わない。食品に含まれる成分でもあり、46通知の規制対象から新制度は除外されている。46通知の『専ら医薬品リスト』から外すことを検討してもよい成分もあり、次の規制改革会議では食薬区分の見直しも申し送り事項としたい。制度の狭間の問題を解決しないといけない」
――受理件数(300件)に対する評価は。
「少なすぎる。年内に1000商品は必要ではないか」
※規制改革会議は、7月の参院選後、新たな会議体として発足する予定。