消費者庁でサプリメントの定義に関する検討が始まった。境界があいまいな「サプリメント」の対象範囲を形状からどこに定めるかが焦点になる。利用目的、成分特性、製造管理の観点を踏まえ、一体的に検討する。機能性表示食品等と同様、サプリメントに対する健康被害報告、GMP(適正製造規範)の義務化を念頭に置くとみられる。
 サプリメントに対する規制は、厚生労働省が営業許可制の要否、健康被害報告について検討する。消費者庁は、定義、製造管理の在り方を検討する。消費者庁は11月27日、食品衛生基準審議会の第1回会合を開き、健康食品関連の業界5団体からヒアリングを行った。次回会合では、消費者団体からヒアリングを行う。
サプリメントに対する規制は、厚生労働省が営業許可制の要否、健康被害報告について検討する。消費者庁は、定義、製造管理の在り方を検討する。消費者庁は11月27日、食品衛生基準審議会の第1回会合を開き、健康食品関連の業界5団体からヒアリングを行った。次回会合では、消費者団体からヒアリングを行う。
米国のサプリメントは①目的(通常の食事の補完)②形状(カプセル・錠剤等)③成分(ビタミン、ミネラル、ハーブ等)の3要件で定義される。難しいのは、「形状」だ。健康機能を表示するグミやチョコ、ガム、飴、クッキーなど、一般食品にあたる領域で形状は多様化している。
機能性表示食品制度では、「天然由来の抽出物、化学的反応等により天然物と成分割合の異なる成分、化学的合成品を原料とする錠剤、カプセル剤、粉末剤、液剤」などと規定されている。GMPの義務化などを行うため制度の運用上定められている定義。ただ、「いわゆる健康食品を含むサプリメント全般の実態を踏まえたものではなく、ありきの議論ではない」(消費者庁)とする。
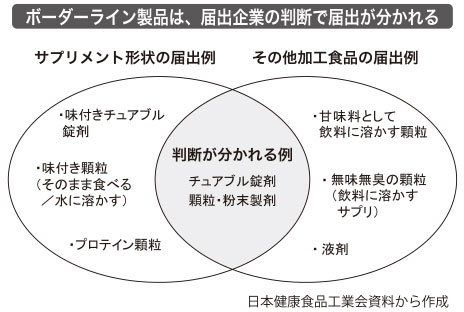
機能性表示食品の届出における区分も企業判断が分かれる。サプリメント形状の届出例は、味付きのチュアブル錠剤や顆粒、同様の形状でも無味無臭の顆粒は「その他加工食品」として届出例がある。
業界団体からは、サプリメントの対象を無味無臭であるなど外観から成分の変質、異物混入に気づきにくいものに絞ることを求める意見があった。一方、委員は幅広く網をかけることを求めた。「無味無臭で線引きすると、健康機能をうたうグミは味をつけてはいけないことになる」と部会長も否定的な見方を示した。
「目的」も争点になる。ヒアリングでは複数の団体が、サプリメントについて「健康の維持・増進に資するもの」と触れた。これに委員から「健康機能を訴求するなら一定の科学的根拠が必要」、「サプリメントを対象にした制度化が必要」との指摘があった。サプリメントは、保健機能食品、「いわゆる健康食品」をまたぎ横串で利用される形状で複雑な構造。形状のみを対象にした制度設計は慎重な検討が必要だ。
定義に対してはほかに①特定成分の濃縮物であること(過剰摂取のリスク)、②食経験が少ないこと、③賦形剤(錠剤の成形等に利用される添加剤)の品質などに着目した検討が必要との意見があった。業界団体は、「過剰摂取の問題は注意表示、啓発で対応すべき」(健康食品産業協議会)と指摘した。
品質管理のためのGMPは、紅麹事件を受け、機能性表示食品、トクホは義務化された。一方で「いわゆる健康食品」は、国が「望ましい」と示すだけにとどまる。サプリメントの区分が明確でないため規制が難しい。
GMPの義務化は、多くの業界団体が「対応可能」との認識を示した。一方で、菓子類など一般食品と同一の製造ラインで製造する事業者も多い。HACCPとの二重規制で製造企業の負担は増える。
また、海外はGMP義務化で先行するが、各国規制で内容はばらつきがある。輸入原材料への国内GMP準拠も困難との見解を示した。
サプリの定義の行方
安全性の観点重視
部会長「国民目線で」繰返す
消費者庁・食品衛生基準審議会の議論は、サプリメントに対する厳しい議論が予想される。部会長の曽根博仁新潟大学院医歯学総合研究科教授も初会合からも指摘が相次いだ。
機能性表示食品制度に対しては、「経済優先の敷居の低い仕組みで取り入れられた結果、科学的根拠が不十分なものが入り全体の信頼性がゆらいだ」と評価。紅麹事件にも「機能性表示食品全体に問題があるかのような誤認がある一方、制度の問題点も多くの有識者から指摘された。有効性のエビデンスの水準を高める必要ある」と、見直しが必要との認識を示した。
「健康の維持・増進に資する」というサプリメントの目的には、「国民の一人としてフレーズが期待を与える。すっきりさわやか程度であればよいが、血糖値が高めの方に、肥満の方にとなると自由に言わせてくれというのはいかがなものか」、「副作用がないため効果を期待して摂りすぎる。健康被害もある中で有効性、品質管理まで一体的に考えないといけない」と触れた。
健康被害のリスクには、「薬は飲み過ぎると副作用が起こると認識している。一方で健食は食べ過ぎる。グミはおいしく効能への期待より習慣として口に入れる傾向もある。濃縮成分なら過量摂取も注意しないといけない」、「多くの国民は薬と区別がつかない。誤認されるものと認識しないといけない」と指摘した。
健康食品は、原材料の多くを海外に依存する。輸入原材料に対する国内GMP準拠にハードルがあることには、「国民目線なら、輸入原料を使わないでという率直な感想を持たれる。輸入だから免責ととられないよう考えないといけない」、「日本で日本人が安心して食べられる。国内GMPをすべて適用させるのが難しい実務の状況はあるだろうが、各国がしないといけないこと。日本市場が無視され、成長産業がダメになるという認識ではなく、優先順位として安全性のため何をすべきか追求する姿勢でお願いしたい」と要求した。
サプリ・業界団体の見解
定義の意見集約がカギ
消費者庁のサプリメントに関する検討会は、業界5団体からヒアリングした。定義に対する考えに大きな違いはなく、GMP(適正製造規範)の義務化は必要との考えを示す。団体の足並みが揃うか重要になる。
定 義
CRN JAPAN(日本栄養評議会)
①形状、②健康の維持・増進に役立つことをうたう食品、③風味を有さない、④過剰摂取など健康被害の発生のおそれがある――の4要件を提案。過剰摂取は、目安量表示等で対応。通常の加工食品は除く。
日本健康食品工業会
①形状による適否、②目的(栄養補助、機能性付与)、③過剰摂取リスク(通常食品と異なる摂取行動)、④GMP準拠の可否――の4要件。
日本健康・栄養食品協会
特段の提案なし。
日本健康食品規格協会
①目的(健康の維持・増進に資するものとして食事を補充する)、②成分、③形状(一定量を日常的に摂取可能とすることを意図した剤型)――の3要件を考慮。形状は、社会通念上、容易に通常食品と認識されるものは除く。また、「成分」は、外観等から品質の良否の判断が難しく、高用量の成分摂取、通常の食経験を逸脱した方法による成分摂取が可能なため、安全性を考慮。
健康食品産業協議会
①形状、②健康の維持・増進に役立つことをうたう食品、③風味を有さない、④健康被害の発生のおそれがある食品――の4要件。CRN JAPAN同様、風味を楽しむものは除く。
GMP
CRN JAPAN
原料はHACCPを徹底。輸入原料はGMPによる管理は困難。サプリメントはGMPを義務化するが、グミ、ゼリーなど一部剤型は、人員・設備の面から実効性確保のため除く。
日本健康食品工業会
一定のチャレンジはあるが準備期間が確保されれば対応は現実的。
日本健康・栄養食品協会
原材料の過剰摂取、HACCP、広告(パッケージ)を一体的に検討する必要性がある。
日本健康食品規格協会
過剰摂取など通常食品と異なるリスクを念頭に、海外はGMP義務化されており必要。サプリメント固有の制度の必要性にも言及。
健康食品産業協議会
輸入品に国内GMP準拠を求める原料製造への導入は困難。国内原料製造はHACCPで十分。人員等への投資が難しい。また、グミなど食品とサプリメントの専用製造ライン設置等はコスト増。現状は入れ替え対応のため、形状により区分。
消費者庁でサプリメントの定義に関する検討が始まった。境界があいまいな「サプリメント」の対象範囲を形状からどこに定めるかが焦点になる。利用目的、成分特性、製造管理の観点を踏まえ、一体的に検討する。機能性表示食品等と同様、サプリメントに対する健康被害報告、GMP(適正製造規範)の義務化を念頭に置くとみられる。
米国のサプリメントは①目的(通常の食事の補完)②形状(カプセル・錠剤等)③成分(ビタミン、ミネラル、ハーブ等)の3要件で定義される。難しいのは、「形状」だ。健康機能を表示するグミやチョコ、ガム、飴、クッキーなど、一般食品にあたる領域で形状は多様化している。
機能性表示食品制度では、「天然由来の抽出物、化学的反応等により天然物と成分割合の異なる成分、化学的合成品を原料とする錠剤、カプセル剤、粉末剤、液剤」などと規定されている。GMPの義務化などを行うため制度の運用上定められている定義。ただ、「いわゆる健康食品を含むサプリメント全般の実態を踏まえたものではなく、ありきの議論ではない」(消費者庁)とする。
機能性表示食品の届出における区分も企業判断が分かれる。サプリメント形状の届出例は、味付きのチュアブル錠剤や顆粒、同様の形状でも無味無臭の顆粒は「その他加工食品」として届出例がある。
業界団体からは、サプリメントの対象を無味無臭であるなど外観から成分の変質、異物混入に気づきにくいものに絞ることを求める意見があった。一方、委員は幅広く網をかけることを求めた。「無味無臭で線引きすると、健康機能をうたうグミは味をつけてはいけないことになる」と部会長も否定的な見方を示した。
「目的」も争点になる。ヒアリングでは複数の団体が、サプリメントについて「健康の維持・増進に資するもの」と触れた。これに委員から「健康機能を訴求するなら一定の科学的根拠が必要」、「サプリメントを対象にした制度化が必要」との指摘があった。サプリメントは、保健機能食品、「いわゆる健康食品」をまたぎ横串で利用される形状で複雑な構造。形状のみを対象にした制度設計は慎重な検討が必要だ。
定義に対してはほかに①特定成分の濃縮物であること(過剰摂取のリスク)、②食経験が少ないこと、③賦形剤(錠剤の成形等に利用される添加剤)の品質などに着目した検討が必要との意見があった。業界団体は、「過剰摂取の問題は注意表示、啓発で対応すべき」(健康食品産業協議会)と指摘した。
品質管理のためのGMPは、紅麹事件を受け、機能性表示食品、トクホは義務化された。一方で「いわゆる健康食品」は、国が「望ましい」と示すだけにとどまる。サプリメントの区分が明確でないため規制が難しい。
GMPの義務化は、多くの業界団体が「対応可能」との認識を示した。一方で、菓子類など一般食品と同一の製造ラインで製造する事業者も多い。HACCPとの二重規制で製造企業の負担は増える。
また、海外はGMP義務化で先行するが、各国規制で内容はばらつきがある。輸入原材料への国内GMP準拠も困難との見解を示した。
サプリの定義の行方
安全性の観点重視
部会長「国民目線で」繰返す
消費者庁・食品衛生基準審議会の議論は、サプリメントに対する厳しい議論が予想される。部会長の曽根博仁新潟大学院医歯学総合研究科教授も初会合からも指摘が相次いだ。
機能性表示食品制度に対しては、「経済優先の敷居の低い仕組みで取り入れられた結果、科学的根拠が不十分なものが入り全体の信頼性がゆらいだ」と評価。紅麹事件にも「機能性表示食品全体に問題があるかのような誤認がある一方、制度の問題点も多くの有識者から指摘された。有効性のエビデンスの水準を高める必要ある」と、見直しが必要との認識を示した。
「健康の維持・増進に資する」というサプリメントの目的には、「国民の一人としてフレーズが期待を与える。すっきりさわやか程度であればよいが、血糖値が高めの方に、肥満の方にとなると自由に言わせてくれというのはいかがなものか」、「副作用がないため効果を期待して摂りすぎる。健康被害もある中で有効性、品質管理まで一体的に考えないといけない」と触れた。
健康被害のリスクには、「薬は飲み過ぎると副作用が起こると認識している。一方で健食は食べ過ぎる。グミはおいしく効能への期待より習慣として口に入れる傾向もある。濃縮成分なら過量摂取も注意しないといけない」、「多くの国民は薬と区別がつかない。誤認されるものと認識しないといけない」と指摘した。
健康食品は、原材料の多くを海外に依存する。輸入原材料に対する国内GMP準拠にハードルがあることには、「国民目線なら、輸入原料を使わないでという率直な感想を持たれる。輸入だから免責ととられないよう考えないといけない」、「日本で日本人が安心して食べられる。国内GMPをすべて適用させるのが難しい実務の状況はあるだろうが、各国がしないといけないこと。日本市場が無視され、成長産業がダメになるという認識ではなく、優先順位として安全性のため何をすべきか追求する姿勢でお願いしたい」と要求した。
サプリ・業界団体の見解
定義の意見集約がカギ
消費者庁のサプリメントに関する検討会は、業界5団体からヒアリングした。定義に対する考えに大きな違いはなく、GMP(適正製造規範)の義務化は必要との考えを示す。団体の足並みが揃うか重要になる。
定 義
CRN JAPAN(日本栄養評議会)
①形状、②健康の維持・増進に役立つことをうたう食品、③風味を有さない、④過剰摂取など健康被害の発生のおそれがある――の4要件を提案。過剰摂取は、目安量表示等で対応。通常の加工食品は除く。
日本健康食品工業会
①形状による適否、②目的(栄養補助、機能性付与)、③過剰摂取リスク(通常食品と異なる摂取行動)、④GMP準拠の可否――の4要件。
日本健康・栄養食品協会
特段の提案なし。
日本健康食品規格協会
①目的(健康の維持・増進に資するものとして食事を補充する)、②成分、③形状(一定量を日常的に摂取可能とすることを意図した剤型)――の3要件を考慮。形状は、社会通念上、容易に通常食品と認識されるものは除く。また、「成分」は、外観等から品質の良否の判断が難しく、高用量の成分摂取、通常の食経験を逸脱した方法による成分摂取が可能なため、安全性を考慮。
健康食品産業協議会
①形状、②健康の維持・増進に役立つことをうたう食品、③風味を有さない、④健康被害の発生のおそれがある食品――の4要件。CRN JAPAN同様、風味を楽しむものは除く。
GMP
CRN JAPAN
原料はHACCPを徹底。輸入原料はGMPによる管理は困難。サプリメントはGMPを義務化するが、グミ、ゼリーなど一部剤型は、人員・設備の面から実効性確保のため除く。
日本健康食品工業会
一定のチャレンジはあるが準備期間が確保されれば対応は現実的。
日本健康・栄養食品協会
原材料の過剰摂取、HACCP、広告(パッケージ)を一体的に検討する必要性がある。
日本健康食品規格協会
過剰摂取など通常食品と異なるリスクを念頭に、海外はGMP義務化されており必要。サプリメント固有の制度の必要性にも言及。
健康食品産業協議会
輸入品に国内GMP準拠を求める原料製造への導入は困難。国内原料製造はHACCPで十分。人員等への投資が難しい。また、グミなど食品とサプリメントの専用製造ライン設置等はコスト増。現状は入れ替え対応のため、形状により区分。